Wie entsteht Krebs?
Umwelteinflüsse, Ernährung, Altern – oder die Gene? Krebs kann ganz unterschiedliche Ursachen haben. Doch immer spielen Proteine eine wichtige Rolle.
Umwelteinflüsse, Ernährung, Altern – oder die Gene? Krebs kann ganz unterschiedliche Ursachen haben. Doch immer spielen Proteine eine wichtige Rolle.
Proteine sind wie kleine Arbeiter im Stoffwechsel, ohne die nichts läuft. Gleichwohl ist alles im Körper genau geregelt, auch welche und wie viele Proteine eine Zelle produziert. Läuft hier etwas schief, kann Krebs entstehen. Dabei unterscheidet man zwischen genetischen und nicht-genetischen Fehlern.
Genetische Veränderungen setzen Krebs in Gang
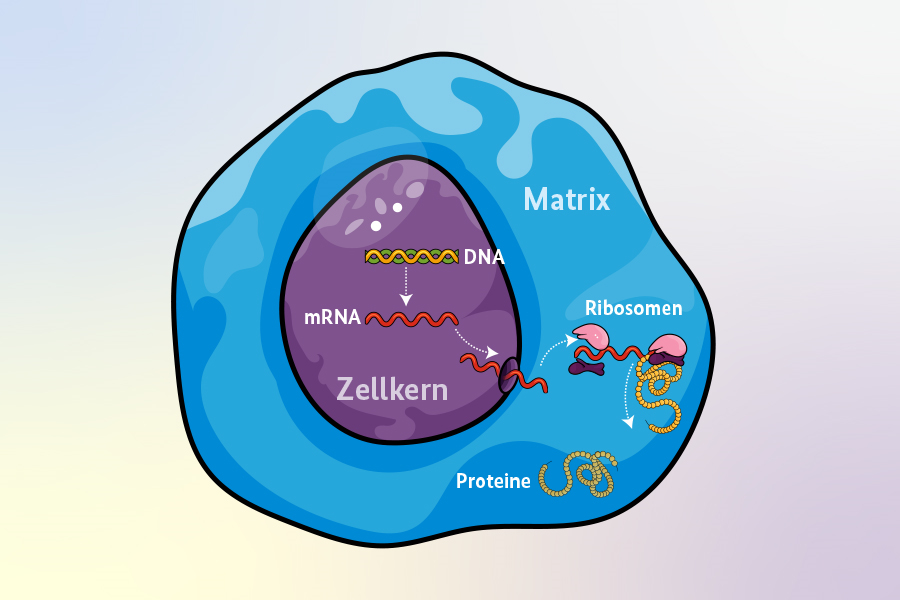
Jede Zelle verfügt über Erbgut, und zwar in Form von DNA in ihrem Zellkern. Man kann sich die DNA als Bauplan des Lebewesens vorstellen: In einzelnen Abschnitten des Planes (den Genen) stehen Bauanleitungen für verschiedene Proteine.

Kommt es zu einem Schreibfehler, beispielsweise durch eine Mutation, verfälscht das die Bauanleitung. Es gibt zwar Reparaturmechanismen, doch nicht immer gelingt es, den Fehler ungeschehen zu machen. Je nach Art und Schwere des Fehlers wird das entsprechende Protein nun falsch aufgebaut und macht seine Arbeit womöglich schlechter oder gar nicht mehr; manchmal wird es aber auch erschreckend produktiv.
Beides kann zu Krebs führen: wenn Proteine, die vor Krebs schützen, nicht mehr oder nur noch schlecht funktionieren. Oder andere, die am Zellwachstum beteiligt sind, plötzlich daueraktiv sind.
Auch nicht-genetische Ursachen führen zu Krebs
Zellen im menschlichen Körper sind sehr unterschiedlich. Eine Leberzelle muss andere Arbeit verrichten als eine Muskel- oder eine Hautzelle und braucht dementsprechend andere Proteine. Die DNA liegt in allen Zellen identisch vor. Damit die unterschiedlichen Zelltypen aus den vielen Genen die richtigen Proteine produzieren, gibt es verschiedene Steuerungsmechanismen.
Manchmal geschehen hierbei auch Fehler.
Fehlerquelle 1: Epigenetik – Zusammenspiel von Genen und Umwelt
Sogenannte epigenetische Markierungen satteln sich auf einzelne Gene auf (griech. Vorsilbe: „epi“ = auf) und können sie stumm- oder freischalten. Dabei handelt es sich um kleine chemische Gruppen, die sich anheften. Sie können wie ein buntes Lesezeichen sein, das „Hierher!“ signalisiert. Daraufhin wird das Gen vermehrt abgelesen. Es gibt aber auch Markierungen, die das Ablesen erschweren oder ganz verhindern. Je nachdem werden die betroffenen Proteine verstärkt, vermindert oder auch gar nicht gebildet.
Im Lebensverlauf kann es durch Umwelteinflüsse, Ernährung, Alterungsprozesse oder viele andere Faktoren zu epigenetischen Fehlern kommen. Wird dadurch ein Gen blockiert, das die Zelle vor Krebs schützt, oder werden umgekehrt Gene vermehrt abgelesen, die das Wachstum beschleunigen, kann das zu einer Krebserkrankung führen.
Fehlerquelle 2: Auf dem Weg vom Gen zum Protein
Ist ein Gen zum Ablesen freigegeben, startet der Prozess: Der erste Schritt, das Ablesen, kann man sich wie einen kleinen Zug vorstellen, der sich an das Gen anheftet und die gesamte Strecke abfährt, wobei er die Informationen aufnimmt. Die Bauanleitung ist aber in einer Sprache geschrieben, welche die kleinen Fabriken, die die Proteine aufbauen (Ribosomen), nicht verstehen.
Daher muss in einem Zwischenschritt in eine andere Sprache übersetzt werden: die messengerRNA (kurz: mRNA). Diese kann dann zu den Proteinfabriken transportiert werden, wo Baustein für Baustein die Proteine aufgebaut werden.
Bei diesem Prozess können eine Reihe von Fehlern passieren, die zu einer Krebserkrankung führen können.
Nicht jeder Tumor ist gleich. Die individuellen genetischen und nicht-genetischen Veränderungen unterscheiden sich von Krebsart zu Krebsart und auch von Mensch zu Mensch. Zu den hier vorgestellten gibt es weitere Fehlermöglichkeiten. Alle zu erfassen und im Detail aufzuklären, ist das tägliche Bestreben der Forschung.
Gezielte Behandlung durch präzise Analyse
Bereits heute können Forschende viele der für Krebs ursächlichen Veränderungen in Zellen analysieren. Hier setzt die Präzisionsmedizin an.
Mit der Endsilbe „-omics“ werden verschiedene Methoden gekennzeichnet, die solche individuellen Veränderungen aufdecken und Hinweise auf die optimale Behandlung geben: Mithilfe von Proteomics lässt sich zum Beispiel das Proteom analysieren, also die Menge und Art der in einer Zelle oder einem Gewebe vorhandenen Proteine. So kann man sehen, welche Wachstumswege Tumorzellen nutzen. Eine Genanalyse (Genomics) spürt Mutationen im Erbgut auf, die zum Krebswachstum beitragen. Das zeigt beispielsweise, ob es sich um familiär vererbbaren Krebs handelt. „Transkriptomics“ erkennen die Gesamtheit der mRNA einer Zelle oder einem analysierten Gewebe. So lässt sich u. a. nachweisen, wie häufig ein Gen abgelesen und in ein Protein umgesetzt wird.
Hoffnung auf bessere Diagnose und Behandlung
Kennt man die Strategien, wie ein Tumor entsteht, lassen sich in vielen Fällen bereits mit modernen Krebsmedikamenten gezielt die Proteine angreifen, die im Krebswachstum eine Rolle spielen.
Die Kenntnis von krebstypischen Proteinen könnte auch die Früherkennung revolutionieren. Ließen sich im Blut Hinweisgeber darauf (Biomarker) mittels einer Liquid Biopsy aufspüren, könnte Krebs zukünftig früher und mithilfe weniger körperlich belastender Methoden entdeckt werden. An der Verlässlichkeit solcher Biomarker-Tests wird derzeit gearbeitet.
Viele Forschungsgruppen bündeln all ihre Energie darin, Krebs besser zu erkennen und zu behandeln oder – noch besser – ihn von vornherein zu verhindern. All dies zum Wohl der Patientinnen und Patienten voranzubringen, ist die Mission der Nationalen Dekade gegen Krebs – damit auch Betroffene mit bislang schwer zu behandelnden Krebserkrankungen eine immer bessere Prognose bekommen.